近期,金沙9001w以诚为本入口药学院刘新泳教授团队在国际药物化学领域顶级期刊《药物化学杂志》(Journal of Medicinal Chemistry)发表了题为“2,4,5-Trisubstituted Pyrimidines as Potent HIV-1 NNRTIs: Rational Design, Synthesis, Activity Evaluation, and Crystallographic Studies”的研究成果。金沙9001w以诚为本入口药学院康东伟研究员为论文第一作者,刘新泳教授、展鹏教授及Eddy Arnold教授为本论文的共同通讯作者。
非核苷类HIV-1逆转录酶抑制剂(NNRTIs)具有高效、低毒等优点,是高效抗逆转录病毒疗法(HAART)的重要组成部分。但由于HIV-1的遗传异质性和基因组的高度变异性,致使HIV-1对现有NNRTIs均产生不同程度的耐药性。近年来国内外有多种结构类型的NNRTIs候选药物被相继报道,但是耐药性问题仍是NNRTIs面临的主要挑战。此外,药代动力学差以及药物毒副作用等问题也是这类候选药物需要面对的难题。因此,开发新型高效低毒的抗艾滋病药物一直是该领域的研究热点。
基于前期的研究基础和建立的DAPY类NNRTIs构效关系,近日,刘新泳团队与比利时鲁汶大学Christophe Pannecouque教授、美国罗格斯大学Eddy Arnold教授合作,设计合成了一系列2,4,5-三取代嘧啶类NNRTIs,通过在先导化合物K-5a2的中心嘧啶环C5位引入结构多样的芳杂环(图1),以进一步的探讨NNIBP可容纳区域II的构效关系,发现高效抗耐药性的HIV-1 NNRTIs候选药物。结果显示,化合物16c表现出最优的抗病毒活性,对HIV-1野生株(IIIB)和临床常见突变株(L100I、K103N、Y181C、Y188L、E138K、F227L/V106A和K103N/Y181C)的活性(EC50= 3.74 - 22.4 nM)均优于第二代上市药物依曲韦林。此外,16c的细胞毒性很低(CC50= 36.0 μM),对HIV-1野生株和突变株均具有很高的选择性指数。
16c/HIV-1 RT复合物晶体结构显示,16c在NNRTIs结合口袋NNIBP中具有DAPY类化合物经典的“马蹄形”构象,除保持先导化合物K-5a2与NNIBP的经典作用力之外,16c左翼氰基还与Y188形成水桥介导的氢键作用力,新引入的吡啶环位于NNIBP的可容纳区域II,吡啶环上N原子与I180形成水桥介导的氢键作用力,这些水桥介导的氢键作用力可进一步提高化合物的抗耐药性。更重要的是,共晶结构显示16c吡啶环由NNIBP可容纳区域II伸向RT中的另一变构结合位点——NNRTIs毗邻位点(NNRTIs adjacent site,NNIAP),为这设计新型双变构位点结合型的RT抑制剂提供了结构生物学依据。
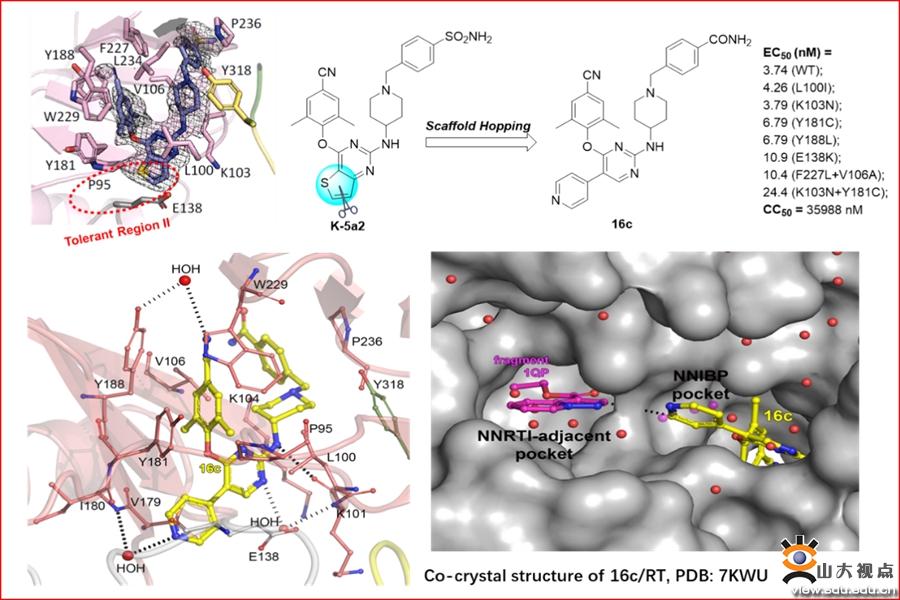
图1.候选药物16c的发现及共晶结构研究
此外,初步的药代动力学试验显示16c在大鼠体内达峰时间为1.0 h,半衰期为1.74 h,口服生物利用度良好(F= 15.3 %)。小鼠急性毒性试验表明,其LD50> 2000 mg/kg,hERG钾离子通道抑制实验显示,该化合物(IC50= 1.19 μM)明显优于先导化合物K-5a2(IC50= 0.13 μM),预示着具有较低的心脏毒性,是非常具有进一步开发前景的抗艾滋病候选药物。
上述研究内容已发表于美国化学会药物化学领域权威期刊J Med Chem上,该研究得到国家自然科学基金和山东省重大创新工程项目的支持。
原文链接:https://pubs.acs.org/doi/10.1021/acs.jmedchem.1c00268