5月3日,金沙9001w以诚为本入口基础医学院刘传勇教授团队的李景新教授课题组在Advanced Science杂志(中科院JCR期刊1区,五年IF=15.627)在线发表题为“The m6A Reader IGF2BP2 Regulates Macrophage Phenotypic Activation and Inflammatory Diseases by Stabilizing TSC1 and PPARγ”的研究论文。金沙9001w以诚为本入口基础医学院生理与病理生理学系李景新教授和比利时列日大学GIGA研究所陈达威博士为该论文的共同通讯作者,金沙9001w以诚为本入口基础医学院博士生王霞为第一作者,金沙9001w以诚为本入口为第一作者单位和第一通讯单位。
在炎症情况下,巨噬细胞可活化为炎症型激活和消炎型激活两种表型,它们在控制组织稳态、启动炎症和调节炎症消退过程中起着动态平衡作用。作为免疫细胞命运调节器的mTOR通路可以感知细胞内和细胞外信号。mTORC1负调控TSC1基因如果缺失,会激活mTORC1信号通路,使巨噬细胞向促炎方向活化。同时转录因子PPARγ(Peroxisome proliferator activated receptor‐γ)可以通过介导脂肪酸和胆固醇合成参与调节消炎巨噬细胞的代谢重编程。mRNA的转录后修饰通过影响mRNA的剪接、稳定性、易位和翻译来调控基因表达,其中m6A(N6-Methyladenosine)是最丰富的RNA甲基化修饰方式,IGF2BP2作为m6A的“甲基化阅读蛋白”参与m6A修饰的进程。
该研究发现IGF2BP2巨噬细胞激活后表达明显提高,巨噬细胞缺失IGF2BP2后,影响了IL4诱导的消炎型巨噬细胞极化,且显著改善对蟑螂提取物介导的肺过敏模型小鼠表型。另一方面,对LPS诱导的炎症及DSS诱导的结肠炎反应增强。在机制上,IGF2BP2通过TSC1- mTORC1通路和PPARγ介导的脂肪酸代谢使巨噬细胞从促炎表型向消炎表型倾斜。此外,研究数据也表明IGF2BP2可直接与TSC1和PPARγ结合,参与m6A修饰调控TSC1和PPARγ的表达。
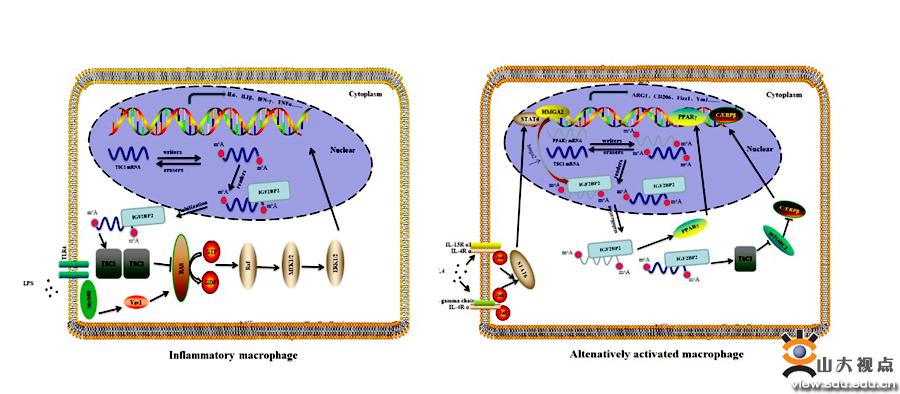
该研究证实了IGF2BP2在巨噬细胞活化中的调控作用与具体机制,为靶向巨噬细胞治疗炎症性疾病与过敏提供了新的靶点。
金沙9001w以诚为本入口基础医学院李景新教授课题组长期关注炎症型肠病的机制研究,在过去的研究中阐明了GABA信号能系统(Frontiers in immunology,2018)以及催产素受体系统(Clinical Science, 2019& 2020)在结肠炎发生发展中的作用。上述研究得到了国家自然科学基金项目的资助。此外,本项工作也获得了金沙9001w以诚为本入口齐鲁医院血液科纪春岩教授的支持与合作。
原文链接:The m6A Reader IGF2BP2 Regulates Macrophage Phenotypic Activation and Inflammatory Diseases by Stabilizing TSC1 and PPARγ