2021-08-07近期,金沙9001w以诚为本入口药学院王凤山教授团队的最新研究成果“Improve Stability of Bioactive Peptides by Enzymatic Modular Synthesis of Peptides withO‑Linked Sialyl Lewis x”在美国化学会期刊ACS catalysis(IF: 13.084)上发表。王凤山教授为该论文的通讯作者,博士生郑小菊为第一作者,金沙9001w以诚为本入口为唯一通讯单位。
多肽具有广泛的生物活性,多肽类药物涉及的治疗领域包括降血糖、抗菌、抗病毒、抗肿瘤、抗新生血管生成、免疫调节等。多肽的分子量介于小分子和蛋白质药物之间,与二者相比其具有活性高、免疫原性低等优势,但多肽有在生理条件下不稳定和受体选择性差等缺陷,所以近年来上市的多肽类药物中经修饰的多肽占比越来越高,其中糖基化修饰是当前多肽类药物研究的点,因为糖链既能增加多肽、蛋白质的稳定性,又能利用糖链的靶向性结合赋予多肽类药物的靶向性。Sialyl Lewis x (sLex)四糖是肿瘤细胞表面的寡糖结构单元,能够与内皮细胞上E-选择素结合,与多肽结合可将其递送至内皮细胞或肿瘤细胞附近。王凤山团队期望建立一种多肽糖基化修饰方法,以实现结合多肽的快速、高效、绿色的糖基化修饰。
本研究建立了一种非常有效的酶法模块化组装策略,实现了多肽的sLex(Siaα2–3Galβ1–4(Fucα1–3)GlcNAcβ1–R)糖基化修饰,合成糖肽的量达到了制备或半制备的规模。该糖基化修饰策略是,在多肽的N端、C端或两个活性多肽的中间,连接上O-糖基转移酶ncOGT能够识别的最短多肽序列VPVSRA,通过多步酶模块化反应连接上sLex。第一个单糖GlcNAc在酶模块化1(EM1)的催化作用下,通过O-糖苷键连接到多肽VPVSRA的Ser上;其它的三个糖分别在酶模块化2、酶模块化3和酶模块化4(EM2−EM4)的作用下,依次连接延长形成sLex四糖。
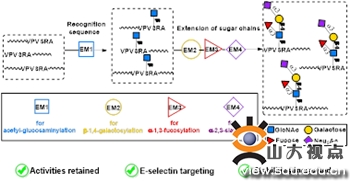
研究选用了两种不同功能的多肽作为模式肽,抗血管生成多肽ES2和抗肿瘤多肽citropin1.1,进行了糖基化修饰。体外HUVEC血管形成实验和抗肿瘤细胞HepG2增殖实验证实,多肽被修饰后其原本的生物学活性没有受到影响。修饰后的糖肽ES2-sLex能与E-选择素结合,在人血清中的半衰期较未修饰的多肽提高了64倍。
王凤山教授课题组研究方向涉及蛋白质、多肽、多糖与寡糖类药物,本论文是将多肽、多糖研究思路与技术相结合的一个结果。这种酶法糖基化修饰活性多肽的策略为多肽的糖基化修饰提供了一个普适的方案,能够使多肽的体内稳定性提高,且能将药物带到靶标部位更好地发挥作用。
本研究获得了2015年省科技重大专项(重大关键技术)和科技部“科技助力经济2020”重点专项资助的支持。
论文链接:https://pubs.acs.org/doi/10.1021/acscatal.1c00955