近日,实验畸形学教育部重点实验室龚瑶琴教授团队和孙龚萍教授团队在CUL4B功能研究方面取得了系列新进展,研究成果先后发表于Cell Death & Differentiation(中科院一区,5年影响因子12.896)、Cell Reports(中科院一区,5年影响因子10.99)和Bone Research(中科院一区,5年影响因子16.969),并受邀在Cellular & Molecular Immunology(中科院一区,5年影响因子17.7)发表评述。
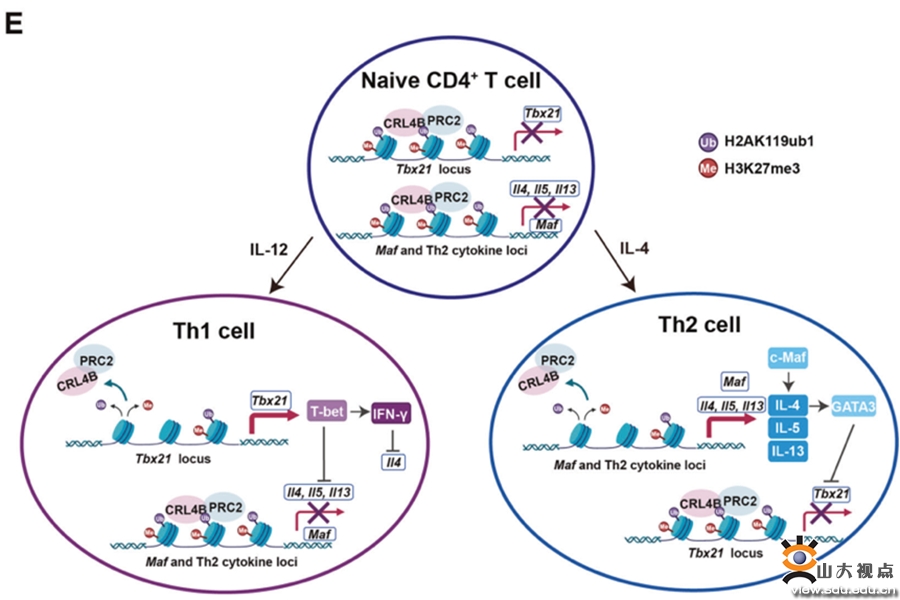
在免疫反应过程中,幼稚CD4+ T细胞可以分化为功能不同的亚群而行使不同的功能,而不同细胞亚群的产生受到转录因子的精准调控,如Th1细胞的分化受转录因子T-bet(由Tbx21基因编码)调控,而Th2细胞的分化受GATA3和c-Maf(由Maf基因编码)调控。而转录因子的谱系特异性表达又受到包括DNA甲基化和组蛋白修饰等表观遗传调控。课题组前期研究显示,CUL4B复合物可以通过单泛素化H2AK119而发挥表观调控作用。为探讨CUL4B介导的组蛋白修饰在调控CD4+ T细胞分化中的作用,课题组构建了T细胞特异性Cul4b基因敲除小鼠模型。结果发现,特异性敲除T细胞CUL4B显著增加Th1和Th2细胞分化、增强Th1和Th2细胞的可塑性、加重了Th2细胞介导的哮喘表型,说明CUL4B对于限制Th1和Th2过度分化是必不可少的。机制研究发现,CUL4B复合物通过抑制谱系特异性转录因子Tbx21和Maf表达从而抑制Th1和Th2细胞的分化。在Th细胞分化过程中,CUL4B复合物促进Tbx21和Maf基因启动子区域的H2AK119单泛素化,并协同多梳抑制复合物2 (PRC2)促进该区域的H3K27三甲基化,从而抑制Tbx21和Maf的表达。本研究首次揭示了CUL4B复合物介导的H2AK119单泛素化修饰在Th细胞分化过程中的重要作用,拓展了对Th细胞分化表观遗传调控机制的认识。相关研究发表于Cell Death & Differentiation,基础医学院博士研究生秦丽萍为本文的第一作者,龚瑶琴教授和学院教授李培山为本文的共同通讯作者,基础医学院为第一和通讯作者单位。
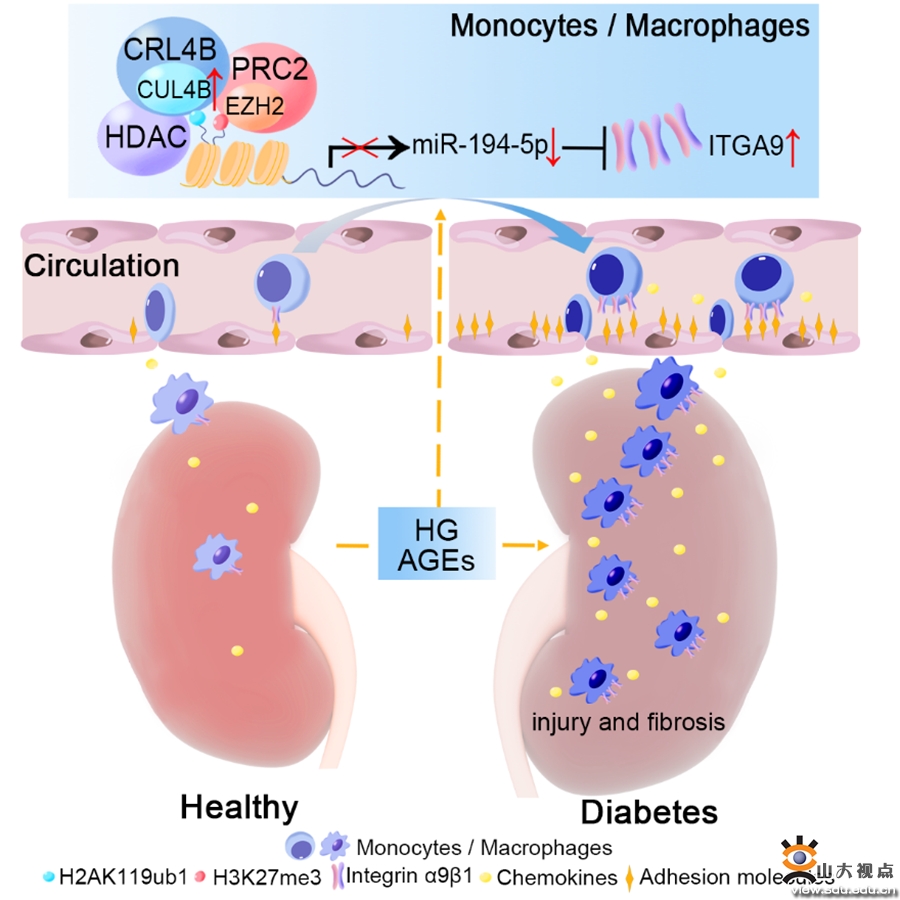
糖尿病肾病(DKD)是糖尿病最常见、最严重的并发症,也是导致终末期肾病的主要原因。近年来的研究显示,巨噬细胞浸润和活化是DKD发生发展的关键。因此,寻找调控肾脏巨噬细胞浸润的关键分子对于DKD的机制研究和干预十分重要。课题组研究发现高糖诱导巨噬细胞CUL4B上调,提示CUL4B可能通过调控巨噬细胞而在DKD发生发展中发挥重要作用。为此,课题组利用诱导性(链脲佐菌素注射加高脂饮食)和自发糖尿病肾病(db/db)模型,分析了髓系细胞特异性敲除CUL4B对DKD的影响,发现髓系细胞缺失CUL4B显著改善糖尿病诱导的肾损伤和纤维化。体内和体外实验分析发现,缺失CUL4B抑制巨噬细胞的迁移、粘附和向肾脏浸润。机制研究显示,CUL4B复合物通过抑制miR-194-5p的表达进而上调整合素α9(ITGA9)的表达,从而促进巨噬细胞的迁移和粘附。该研究揭示CUL4B/miR-194-5p/ITGA9轴是糖尿病肾脏中巨噬细胞浸润的重要调节机制,并可能作为延缓DKD进展的干预靶点。相关研究结果发表于Cell Reports,基础医学院博士研究生金士琦和博士后宋煜为本文的共同第一作者,孙龚萍教授和金沙9001w以诚为本入口齐鲁医院肾内科主任医师刘广义为本文的共同通讯作者,基础医学院为第一作者和通讯作者单位。
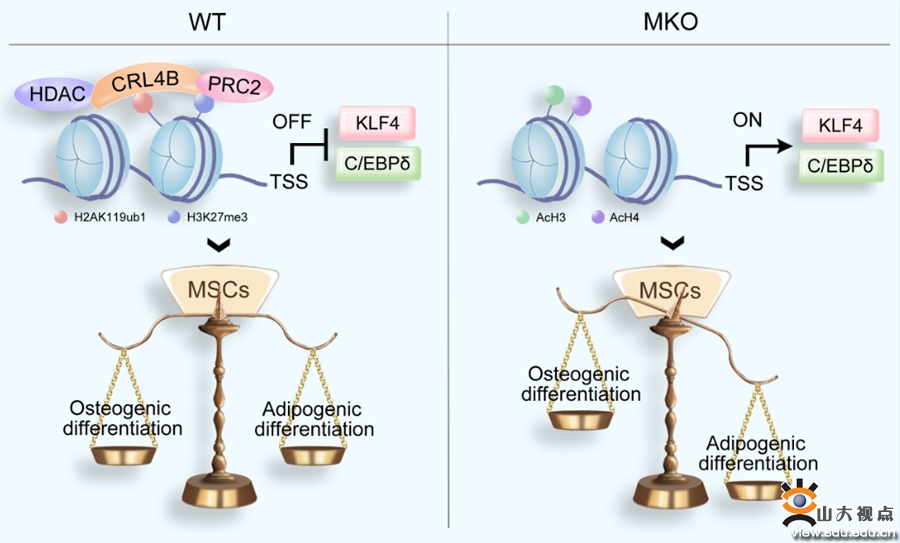
间充质干细胞(mesenchymal stem cells, MSCs)是一类具有自我更新和多向分化潜能的成体干细胞,可以分化为成骨细胞、成软骨细胞和脂肪细胞等。研究显示,作为成骨细胞和脂肪细胞共同的前体细胞,MSCs的成脂分化和成骨分化是相互拮抗的。成脂分化增强会抑制成骨分化,导致骨形成不足;相反,成骨分化增强也会抑制成脂分化。在正常情况下,MSCs向成骨细胞和脂肪细胞分化保持动态平衡。一旦这种平衡被打乱,将会引起一些发育缺陷和代谢相关疾病。课题组前期研究发现,CUL4B突变患者具有身材矮小、短指和肥胖等表型,提示CUL4B可能通过调控MSCs分化而影响以上表型。为此,课题组构建了MSCs特异性Cul4b基因敲除小鼠模型,结果发现,MSCs中缺失CUL4B导致小鼠出生后骨骼发育受损,表现为骨量减少和骨生成减少。在自然衰老和卵巢切除术两种骨质疏松症模型中,MSCs中缺失CUL4B加剧了骨丢失和骨髓脂肪组织积累。细胞学分析发现,CUL4B促进骨髓MSCs成骨分化、抑制其成脂分化。机制分析发现,CUL4B复合物协同PRC2复合物与HDACs复合物,通过促进Klf4和Cebpd基因启动子区域的H2AK119单泛素化、H3K27三甲基化以及H3和H4去乙酰化来抑制Klf4和Cebpd的转录。本研究确立了CUL4B在MSC谱系分化中的关键作用,揭示了间充质干细胞成骨/成脂分化中一种新的表观遗传学调控机制。CUL4B作为骨保护因子发挥作用,表明CUL4B是骨质疏松症治疗的潜在靶点。该研究发表于Bone Research,基础医学院博士研究生于瑞祺为本文的第一作者,龚瑶琴教授和蒋百春副教授为本文的共同通讯作者,基础医学院为第一作者和通讯作者单位。
鉴于课题组在CUL4B复合物调控免疫细胞分化和功能方面取得的多项新进展,Cellular & Molecular Immunology杂志邀请龚瑶琴教授团队针对本领域研究进展撰写评述,系统介绍了CUL4B复合物在调控T细胞、巨噬细胞、髓系来源抑制细胞(MDSCs)分化和功能中的研究进展,为后续研究CUL4B在其他类型免疫细胞中的作用及CUL4B复合物调控炎症性疾病和肿瘤免疫的分子机制提供新思路。基础医学院博士后宋煜为本文的第一作者,龚瑶琴教授和孙龚萍教授为本文的共同通讯作者,基础医学院为第一作者和通讯作者单位。
相关链接:
1.CRL4B complex-mediated H2AK119 monoubiquitination restrains Th1 and Th2 cell differentiation
2.Depletion of CUL4B in macrophages ameliorates diabetic kidney disease via miR-194-5p/ITGA9 axis
3.CUL4B orchestrates mesenchymal stem cell commitment by epigenetically repressing KLF4 and C/EBPδ
4.Cullin 4B-RING E3 ligase complex in immune cell differentiation and function