近日,药学院姜新义教授团队与以色列希伯来大学、金沙9001w以诚为本入口齐鲁医院等多家单位合作,揭示了调控巨噬细胞胆固醇代谢治疗脑胶质瘤的免疫学分子机制,构建了可喷涂水凝胶递药系统,成功应用于胶质母细胞瘤术后免疫治疗。相关研究成果以“Intracavitary Spraying of Nanoregulator‐Encased Hydrogel Modulates Cholesterol Metabolism of Glioma-Supportive Macrophage for Postoperative Glioblastoma Immunotherapy”为题,发表在Advanced Materials。姜新义教授、张彩教授、赵坤教授与陈晨为本文通讯作者,博士研究生董源敏、张晶为共同第一作者,金沙9001w以诚为本入口药学院为第一作者和独立通讯作者单位。
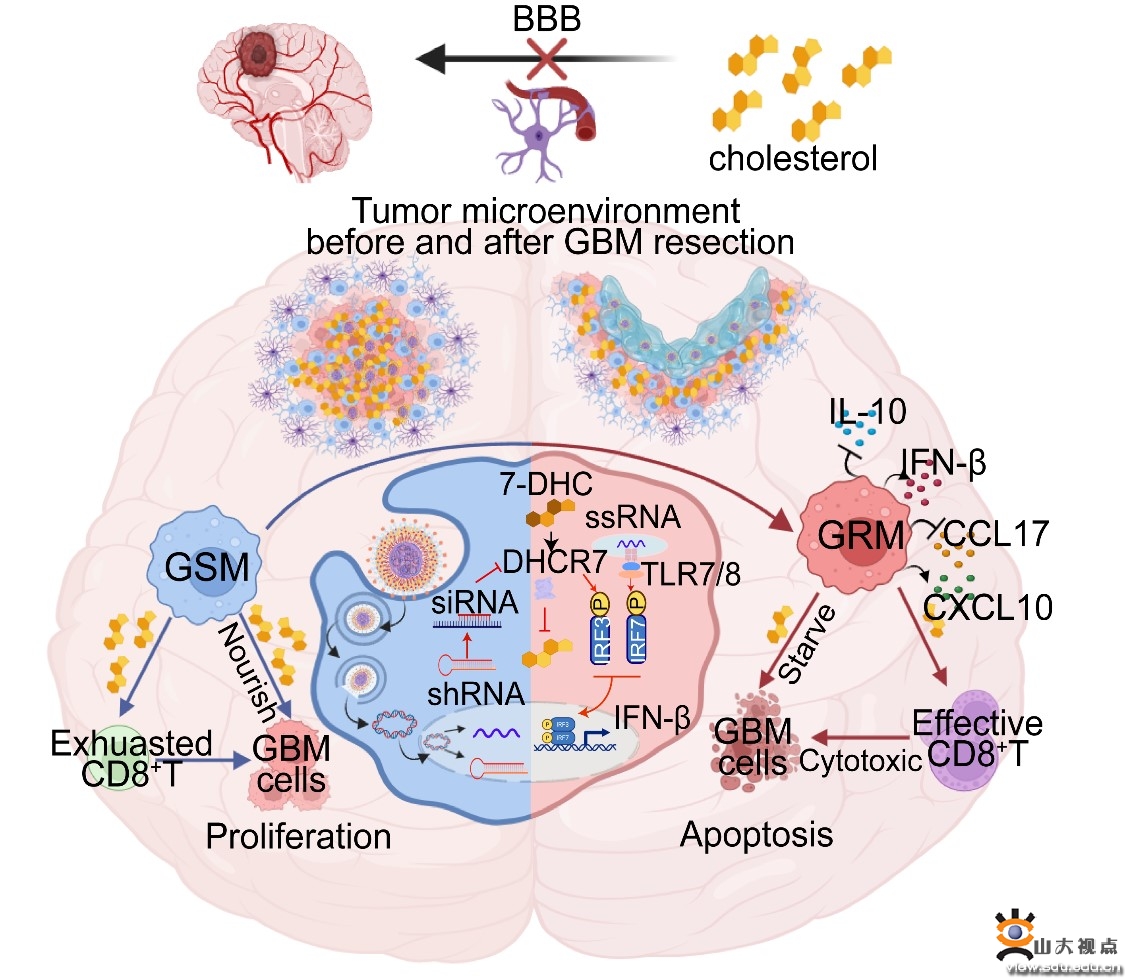
多形性胶质母细胞瘤(GBM)是恶性程度最高的中枢神经系统肿瘤,预后不佳、术后复发率高。中枢神经系统具有独特的胆固醇代谢微环境,GBM细胞生存所需胆固醇主要依赖外源性供应而非自身合成。最新研究表明,肿瘤微环境中胆固醇的代谢失调在肿瘤发生发展及免疫逃逸中发挥关键作用。肿瘤支持型巨噬细胞具有较高的胆固醇外排活性,为肿瘤生长提供所需胆固醇,同时,胆固醇代谢重编程可促进其向促肿瘤表型极化。胶质瘤支持型巨噬细胞(GSMs)是肿瘤微环境最丰富的非肿瘤细胞类型,手术切除引起的炎症导致大量GSMs富集于瘤腔周围,维持免疫抑制微环境并促进肿瘤复发。因此,深入研究GSMs胆固醇代谢特征以及代谢失调导致免疫抑制微环境形成的机制,将有助于开发高效的胶质母细胞瘤靶向免疫新疗法。
团队研究发现,GBM组织内的胆固醇水平异常升高,显著诱导CD8+ T细胞耗竭,而GSMs清除可有效降低胆固醇水平,恢复其杀伤能力。进一步研究证实,GSMs作为胆固醇合成“工厂”,为胶质瘤快速生长提供了重要胆固醇来源。团队通过深入的生物信息学分析和数据挖掘,发现7-脱氢胆固醇还原酶(DHCR7)在GBM患者肿瘤组织中高表达,与患者生存期呈负相关性。DHCR7是一种促进M2型巨噬细胞极化的重要调控因子,并且在GSMs中高表达。因此,研究团队提出通过靶向沉默DHCR7来抑制GSMs中胆固醇的合成,切断胶质瘤细胞的胆固醇供应,有效逆转GBM免疫抑制微环境,遏制术后GBM的复发。
姜新义教授团队与以色列Ofra教授团队合作搭建了“Tumor-on-chip”微流控筛选平台,筛选获得了可高效靶向GSMs的基因递送载体,实现了DHCR7的高效沉默,有效阻断了GSMs胆固醇的合成和供应。shDHCR7与TLR7/8激动剂(ssRNA)联合显著促进GSMs向抗肿瘤表型极化,重塑免疫抑制微环境。为了无缝衔接临床手术治疗方案,研究团队构建了一种以I型胶原蛋白结合肽为基础的可喷涂水凝胶系统,该系统具有优良的生物相容性、可喷涂性、粘附性和药物贮库功能,为GBM术后治疗提供了一种高效递药策略。综上,该研究揭示了GSMs的DHCR7/胆固醇信号在调节免疫抑制微环境中的作用,为临床开展更安全、有效的抗胶质瘤免疫治疗奠定了理论基础和实验依据,具有重要的临床意义及科研价值。
近年来,姜新义教授团队在核酸药物可控递送、治疗性免疫细胞在体编辑等方面取得了一系列重要成果,先后发表于Nature Nanotechnology、Science Translational Medicine、Nature Communications、PNAS、Science Advances、Advanced Materials等期刊。该研究工作得到了国家自然科学基金-国际(地区)合作与交流项目、国家自然科学基金面上项目,山东省自然科学基金-重大基础研究项目,山东省重大科技创新工程项目(2021、2019)等项目支持。
文章链接:https://onlinelibrary.wiley.com/doi/10.1002/adma.202311109