近日,高等医学研究院王维教授团队在Nature communications(中科院一区TOP/JCR Q1,5年IF=17.694)在线发表题为“Structural basis of human SNAPc recognizing proximal sequence element of snRNA promoter”的研究成果。基础医学院青年教师孙建峰、金沙9001w以诚为本入口高等医学研究院博士生李雪为该论文的共同第一作者,基础医学院青年教师孙建峰、美国洛克菲勒大学Robert G. Roeder教授、金沙9001w以诚为本入口高等医学研究院王维教授为共同通讯作者;金沙9001w以诚为本入口为该论文的第一作者单位和通讯作者单位。

在真核生物中,小核RNA(snRNA)在多种细胞基本生命活动中发挥重要作用,如mRNA前体剪接、基因表达调控和核糖体RNA加工。snRNA激活蛋白复合物(SNAPc)特异性识别snRNA启动子的近端序列元件(PSE),并招募RNA聚合酶II或III启动snRNA转录。SNAPc在不同物种中的功能非常保守。但SNAPc如何组装和如何特异性识别PSE序列并调节snRNA转录起始的分子机制尚未清楚。
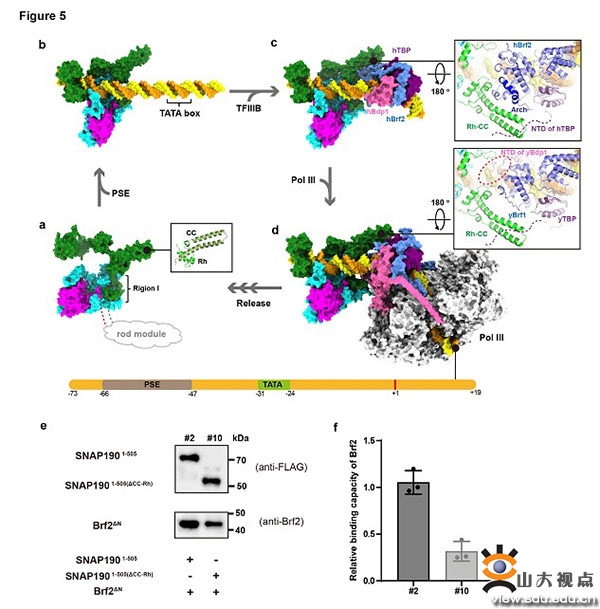
本研究首次以3.49Å的分辨率展示了人源SNAPc核心组分与U6 PSE复合物的冷冻电镜结构。该结构首次揭开了转录因子SNAPc精确分子结构的神秘面纱,详细解释了SNAPc三个核心亚基SNAP190,SNAP50和SNAP43如何组装成高转录活性的mini-SNAPc组件;鉴定出SNAPc特异识别PSE序列的关键残基,解释了mini-SNAPc组件特异性识别U6 PSE的分子机理;综合运用SPR和EMSA等技术手段,系统分析了人源不同snRNA基因的PSE被SNAPc所识别的保守性及兼容性;在已解析结构的基础上,搭建了人源U6启动子的转录起始超级复合物(PIC)装配模型,并鉴定出SNAPc与TFIIIB转录因子互作的关键结构域CC-Rh domain,最终详细解释了Pol III依赖的U6 snRNA转录起始的分子机理。
综上所述,本研究展示了mini-SNAPc/hU6-1 PSE复合物精确的分子模型,不仅解释了U6 snRNA转录起始的分子机理,也为研究SNAPc依赖性启动子(例如U6,H1等)的转录起始复合物组装提供了研究模板,未来可为设计更为高效的siRNA或CRISPR基因编辑系统提供数据支撑。
上述研究得到国家自然科学基金项目、山东省自然科学基金项目的资助。同时特别感谢金沙9001w以诚为本入口药学院侯旭奔教授,自然资源部第三海洋研究所李增鹏教授等的大力支持。
文章链接:https://www.nature.com/articles/s41467-022-34639-1